心血管疾病预防领域正迎来革命性变革。传统风险评估方法主要依赖年龄、血压、血脂等常规临床指标,但这些指标往往在疾病已经形成后才能检测到明显异常。如何在疾病发生前十年甚至更早准确识别高风险人群,一直是临床实践中的难点。

多组学整合的新思路
近年来,随着高通量检测技术的发展,研究者发现血液中的蛋白质和代谢物能够更直接地反映身体的生理状态。这些分子信号不仅受到遗传因素影响,也会随着环境、生活方式和健康状况的变化而动态调整,为长期风险评估提供了全新的信息维度。
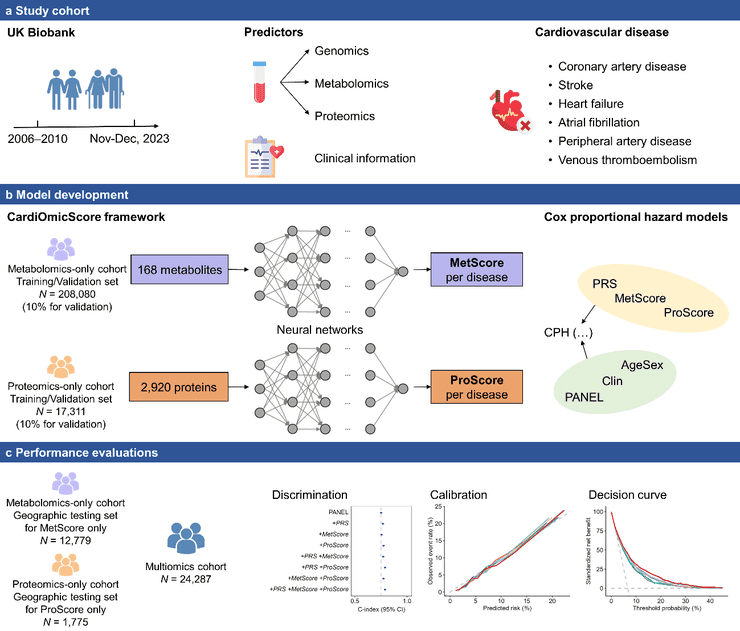
香港大学张清鹏副教授团队的研究创新性地将蛋白组和代谢组信息纳入统一评估框架。研究基于UK Biobank大规模前瞻性队列数据,采用分阶段开发验证的策略,确保了研究结果的可靠性。该研究的一个关键突破是打破了传统"一病一模型"的限制,能够同时评估多种心血管疾病的长期风险。
模型性能的显著优势
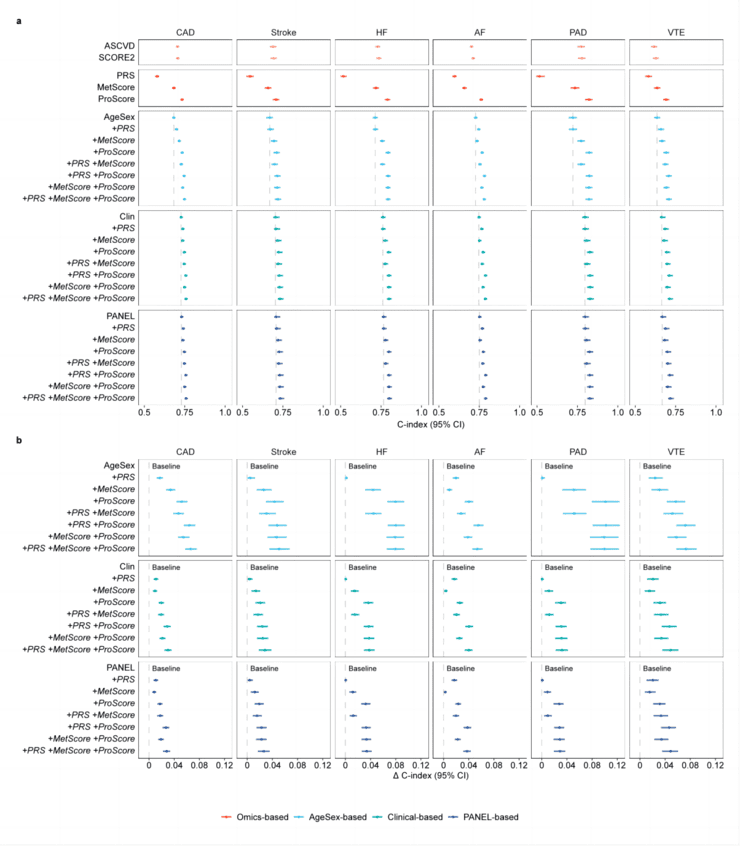
研究团队开发的CardiOmicScore框架分别利用血液中的2,920种蛋白质和168种代谢物训练了两类人工智能模型。结果显示,即使不依赖任何传统临床指标,基于蛋白组的ProScore和基于代谢组的MetScore本身就具备强大的风险识别能力。
ProScore在六种心血管疾病预测中表现最为稳定,其区分高风险与低风险人群的能力明显优于多基因风险评分。在部分心血管结局预测中,ProScore的表现甚至接近常用的临床风险模型。MetScore虽然略逊于ProScore,但整体仍优于遗传风险评估方法。
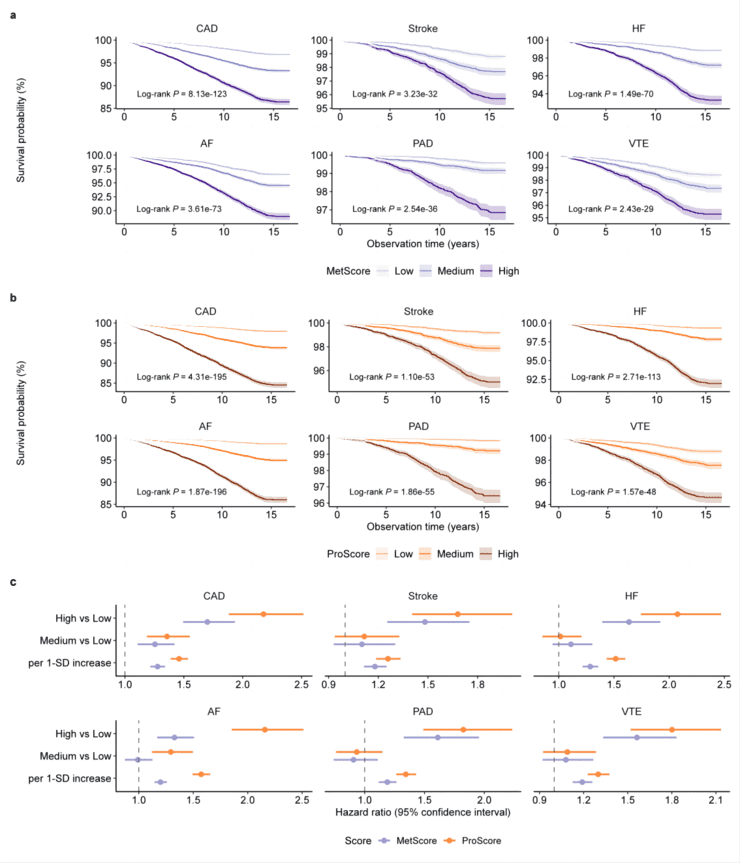
临床应用的增量价值
更重要的是,多组学信息在现有临床评估基础上能提供显著的增量价值。无论模型中已经包含多少临床信息,加入蛋白组或代谢组评分后,预测效果都会得到明显提升。这表明多组学信号反映的是传统临床检查难以直接捕捉的分子层面风险。
从实际应用角度看,这种方法的优势在于能够通过一次血液检测同时评估多种心血管疾病的长期风险。这不仅提高了筛查效率,也更符合临床实践中多种心血管风险往往同时存在的实际情况。
模型的可解释性分析
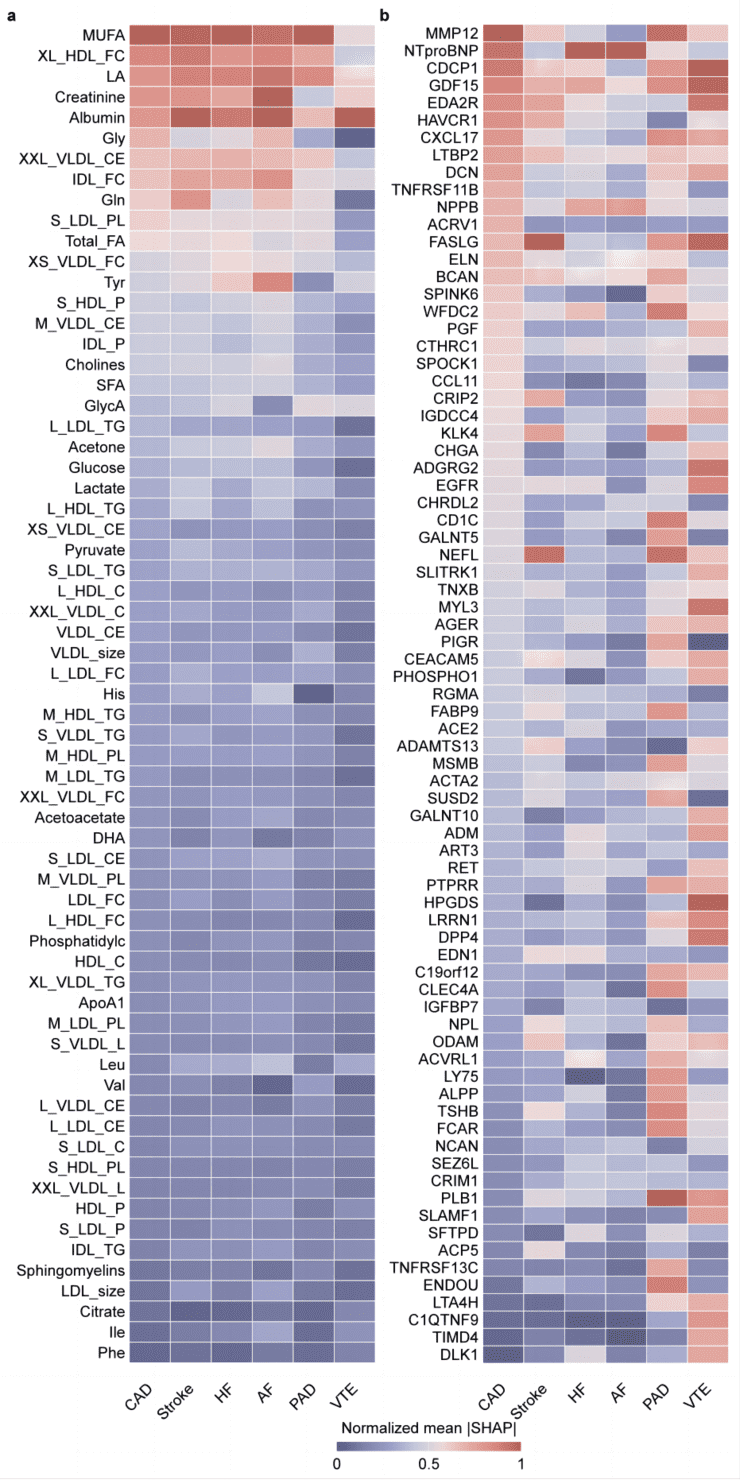
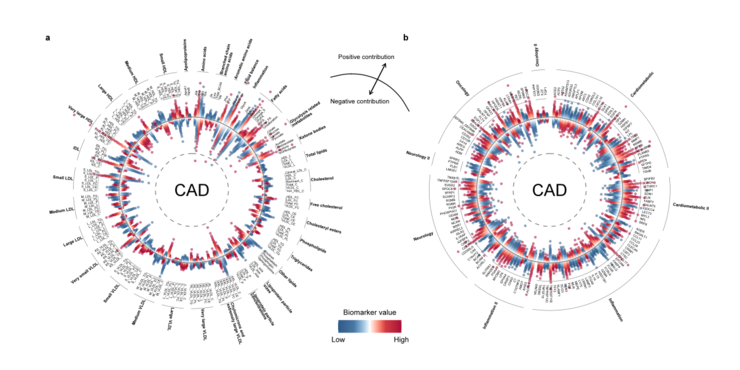
为了理解模型的预测机制,研究团队通过SHAP方法分析了最重要的分子特征。分析结果显示,一些临床上早已熟知的指标仍然是核心预测因子,如与心脏负荷相关的NT-proBNP和NPPB蛋白,以及反映肾功能和营养状态的肌酐和白蛋白。
同时,模型还识别出了一批具有潜在价值的新型生物标志物。在蛋白组中,GDF15、MMP12、FASLG和NEFL显示出较强的预测能力;在代谢组中,谷氨酰胺、脂肪酸、糖蛋白乙酰基(GlycA)以及多种脂质相关分子同样具有重要作用。
这些分子的作用模式与心肌应激、炎症反应和代谢紊乱等已知病理过程高度一致,说明模型确实抓住了心血管疾病的关键生物学信号。
研究设计的严谨性
这项研究的设计体现了高标准的研究方法学要求。研究依托UK Biobank大规模前瞻性队列,采用了"先开发、再验证"的严谨设计。首先利用只包含单一组学信息的大规模人群数据训练模型,随后在独立人群中验证模型效果。
所有疾病结局均通过医院住院记录和死亡登记信息进行确认,确保了结果判定的可靠性。中位随访时间约为15年,使研究能够充分观察心血管疾病的长期发生过程。
技术框架的扩展潜力
CardiOmicScore框架的一个重要特点是具有良好的扩展性。该框架既能学习多种心血管疾病之间的共通生物学特征,也能同时捕捉每一种疾病特有的分子信号。模型输出的是连续的风险评分,而不是简单的二元分类,因此更适合用于长期风险评估。
随着未来进一步整合影像、心电图等多模态数据,这类模型有潜力发展为更全面的心血管风险评估工具。这种方法的另一个优势是能够动态反映风险变化,为个性化干预提供依据。
精准预防的新范式
这项研究为心血管疾病的一级预防提供了新的科学依据。与相对固定的遗传风险不同,蛋白质和代谢物能够反映环境、生活方式和健康状态的综合影响,因此更适合用于动态风险评估和早期干预。
从公共卫生角度,这种方法的推广有望在减少不必要干预的同时,更早、更准确地识别真正的高风险人群。这对于优化医疗资源配置、提高预防效率具有重要意义。
未来研究方向
尽管这项研究取得了显著成果,但仍有一些问题需要进一步探索。例如,不同人群中的预测效果是否存在差异?这些生物标志物在不同种族、年龄组中的表现如何?这些都是未来研究需要重点关注的方向。
此外,如何将这种复杂的多组学评估方法转化为临床可用的检测工具,也是实现实际应用的关键。成本效益分析、标准化检测流程建立等工作都需要持续推进。
行业影响与展望
这项研究代表了医学人工智能发展的一个重要方向——将多组学数据与机器学习算法深度融合,实现对复杂疾病的早期预警和精准预测。这种研究方法不仅适用于心血管疾病,也有望扩展到其他慢性病的风险评估中。
随着检测技术的进步和计算能力的提升,多组学分析的成本正在逐步降低,这为大规模临床应用创造了条件。未来,我们可能会看到更多基于多组学信息的个性化健康管理方案出现。
这项研究的成功也提示我们,在医学人工智能领域,数据质量、研究设计和结果解释同样重要。只有在严谨的科学框架下,人工智能技术才能真正为医疗健康带来实质性改善。