人工智能抗体设计的里程碑事件
2025年12月,生物医药领域迎来历史性突破:Generate Biomedicines公司宣布,其完全由人工智能设计的抗体药物GB-0895正式启动全球Ⅲ期临床试验。这是全球首个从分子设计到临床验证全程由AI驱动的治疗性抗体,其靶点为胸腺基质淋巴细胞生成素(TSLP)——一种在气道炎症反应中扮演“主开关”角色的细胞因子。通过精准阻断TSLP,GB-0895有望为重度哮喘和慢性阻塞性肺疾病(COPD)患者提供革命性治疗方案,尤其针对那些经中高剂量吸入性糖皮质激素仍无法控制病情的难治性患者。
TSLP靶点的治疗价值与GB-0895的差异化优势
TSLP作为炎症级联反应的核心调控因子,长期被视为呼吸道疾病治疗的关键靶点。现有疗法如特泽佩鲁单抗(Tezepelumab)虽已上市,但需每月注射一次,患者依从性面临挑战。GB-0895通过AI优化实现了两大突破性特性:
- 超高亲和力:结合强度较传统抗体提升10倍以上,确保对靶点的完全抑制
- 超长半衰期:约89天的半衰期达到同类药物的3-4倍,用药间隔延长至六个月
这种“一次注射,半年有效”的模式不仅显著降低治疗成本,更从根本上改善患者生活质量。根据Generate Biomedicines披露的数据,在Ⅱ期临床试验中,GB-0895使哮喘急性发作率降低67%,肺功能指标FEV1改善率达32%,且未出现严重不良反应。
从药物发现到药物生成:AI重构研发范式
传统抗体研发依赖耗时费力的试错过程:通过噬菌体展示库筛选数亿个天然分子,或对动物进行免疫后提取抗体,成功率往往低于0.01%。生成式AI的兴起彻底改变了这一格局——制药行业正从“发现”转向“生成”时代。
Generative Biology平台的运作逻辑
Generate Biomedicines的核心技术Generative Biology平台构建了一个“设计-验证-学习”的闭环系统,包含四个迭代阶段:
flowchart LR
A[生成] --> B[构建] --> C[检测] --> D[学习] --> A- 生成阶段:AI算法基于目标特性(如结合强度、稳定性)生成数千种全新蛋白质序列
- 构建阶段:实验室合成这些计算机设计的分子实体
- 检测阶段:高通量自动化平台评估分子的结合力、稳定性和免疫原性
- 学习阶段:实验数据反馈至AI模型,持续优化设计精度
与传统方法最大的区别在于,该平台能同时对多项特性进行协同优化,而非牺牲某一特性换取另一特性。例如在GB-0895设计中,AI同步提升了靶向特异性、血清半衰期和表达产量。
Chroma模型:蛋白质工程的DALL·E
支撑该平台的核心是2022年发布的Chroma模型,其技术架构包含四大创新模块:
- 扩散过程:模拟蛋白质构象的统计热力学特性
- 神经网络架构:实现长程结构推理的次二次方复杂度算法
- 三维合成层:根据残基几何预测快速构建空间结构
- 低温采样算法:优化扩散模型的生成效率
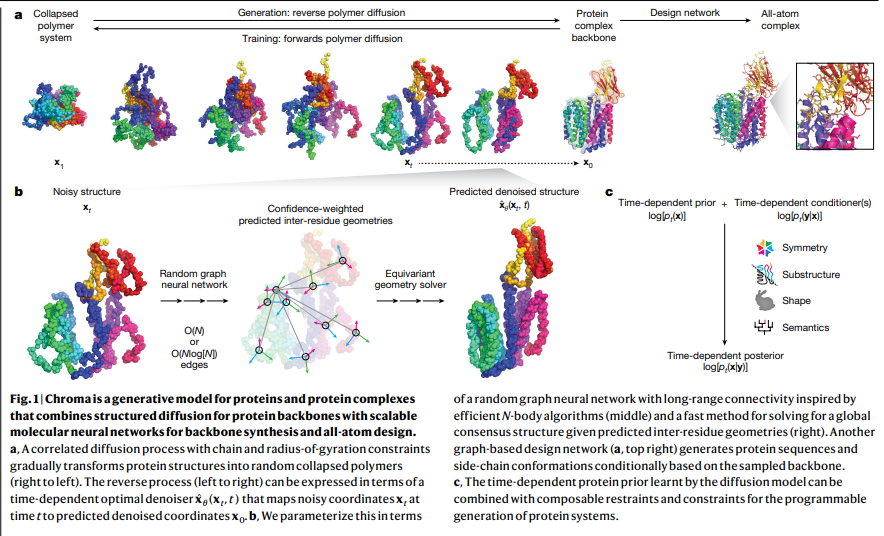 Chroma模型将蛋白质设计转化为带约束的贝叶斯推断过程,支持对称性、亚结构等复杂要求
Chroma模型将蛋白质设计转化为带约束的贝叶斯推断过程,支持对称性、亚结构等复杂要求
通过对310种生成蛋白质的实验验证:
- 92%的分子实现可溶性表达
- 晶体结构与预测模型的RMSD值≤1.2Å
- 两种设计分子达到原子级精度匹配
临床验证与商业布局
SOLAIRIA全球临床试验设计
2025年末启动的SOLAIRIA-1和SOLAIRIA-2试验共纳入1600例12岁以上患者,采用多中心、双盲、安慰剂对照设计。主要终点包括:
| 评估指标 | SOLAIRIA-1 | SOLAIRIA-2 |
|---|---|---|
| 哮喘发作率降幅 | ≥50% | ≥45% |
| FEV1改善率 | ≥30% | ≥25% |
| 急救药物使用量 | 减少≥40% | 减少≥35% |
试验特别设立生物标志物亚组分析,通过检测血清TSLP水平和呼吸道炎症因子,验证AI设计的靶向精确性。初步结果预计在2027年Q2公布。
多元化管线布局
Generate Biomedicines已建立覆盖三大治疗领域的AI研发管线:
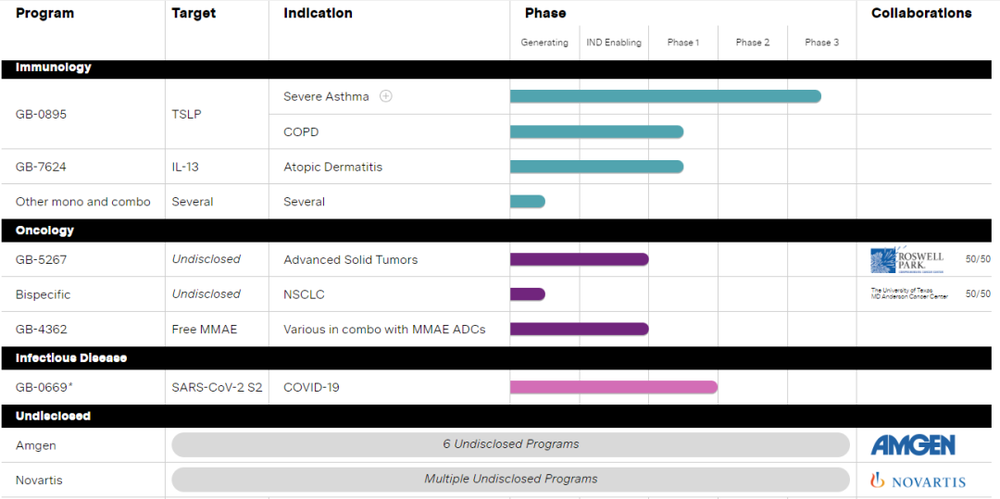 免疫学领域进展最快,肿瘤学合作规模达数十亿美元
免疫学领域进展最快,肿瘤学合作规模达数十亿美元
- 免疫学领域:除GB-0895外,抗IL-13抗体GB-7624已完成临床Ⅰ期。该分子经工程化改造后亲和力达pM级别,半衰期延长至120天,适应症覆盖特应性皮炎和嗜酸性食管炎
- 肿瘤学领域:
- 与MD安德森癌症中心合作开发新一代抗体药物偶联物(ADC),载荷效率提升至95%
- 同诺华合作的未公开靶点多特异性抗体项目,首付款达4.8亿美元
- CAR-T疗法通过AI优化抗原识别域,脱靶毒性降低80%
- 传染病领域:广谱抗病毒蛋白设计项目进入临床前阶段
产业影响与未来挑战
重构制药经济学模型
GB-0895的研发成本较传统模式降低60%,这主要源于:
- 湿实验量减少70%(通过精准的计算机筛选)
- 研发周期压缩50%(四年vs七年)
- 临床失败率预估下降40%(AI优化分子特性)
安进公司研发主管在合作声明中指出:“生成式AI将生物制剂的IND申报时间从5年缩短至18个月,这是本世纪最重大的制药效率革命。”
技术瓶颈与伦理考量
尽管前景广阔,AI抗体设计仍面临三重挑战:
- 数据依赖性:模型需要高质量的结构生物学数据集,而膜蛋白等复杂靶点数据稀缺
- 可解释性:神经网络决策过程如同“黑箱”,监管机构要求提供设计逻辑的生物学合理性证明
- 知识产权:AI生成分子的专利归属尚未形成国际共识
值得关注的是,FDA于2025年发布的《AI生成治疗蛋白指南》首次明确:
“AI工具可作为辅助设计手段,但关键质量属性必须通过传统生物学实验验证”
前瞻:可编程生物学的时代图景
Generate Biomedicines的实践验证了“生物学可编程”假说。随着计算能力的提升(英伟达提供专属超算集群)和算法迭代,未来可能出现更颠覆性的应用场景:
- 动态适应性抗体:根据患者免疫状态实时调整结合亲和力
- 自组装纳米机器:在体内精准定位后释放治疗模块
- 合成免疫系统:通过编程设计实现人工免疫记忆
正如Generate首席执行官Mike Nally所言:“我们正从‘发现自然存在的药物’转向‘创造自然界不存在的疗法’。GB-0895不是终点,而是通向无限可能的起点。”当前,全球已有37家生物技术公司布局AI抗体赛道,预计到2030年,该领域市场规模将突破420亿美元。